
研究背景
糖尿病视网膜病变是糖尿病严重的微血管并发症,可导致不可逆性失明。主要是由高血糖引发小血管管壁增厚,渗透性增加,血管渗漏和闭塞,而由于血管变化,毛细血管内皮开始增殖,缺氧的网膜组织释放出细胞增殖物质,促使形成新生血管,进而导致出血、网膜静脉栓塞,引发糖尿病视网膜障碍。微血管主要由周细胞和内皮细胞组成,周细胞和血管内皮细胞可以通过直接接触和复杂的分子信号联系,共同调节血管的形态和功能。circRNA 已被证实,参与调控多种复杂疾病的发生发展过程,但环状 RNA 在糖尿病引发的视网膜损伤过程中的作用尚不清楚。复旦大学上海医学院附属耳鼻喉眼科医院的颜标研究团队于近日发表在 PNAS 的研究成果揭示了周细胞 - 内皮细胞之间存在外泌体为载体进行信号联系,相关的 circRNA 芯片服务由伯豪生物提供。
研究思路
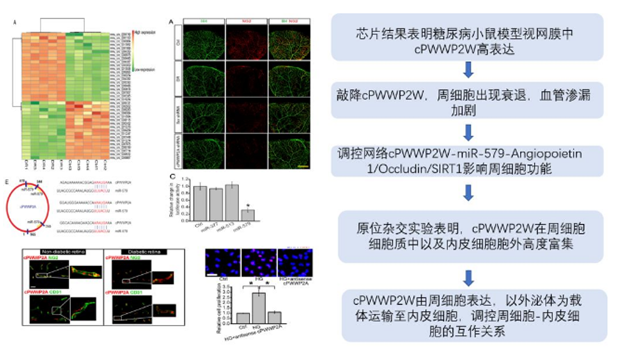
研究结果
circRNA 芯片结果表明,糖尿病小鼠视网膜中 cPWWP2A 高表达,敲降 cPWWP2A, 周细胞数量锐减,微血管渗漏加剧。通过生物信息学分析及荧光素酶报告、pull-down 实验证实,cPWWP2A 可以作为内源性 miR-579 的吸附海绵,促进其靶基因 Angiopoietin1,occludin 和 SIRT1 的表达。调控网络 cPWWP2W-miR-579-Angiopoietin 1/Occludin/SIRT1 对微血管的功能具有重要的调控作用。进一步的研究表明,cPWWP2W 是由周细胞表达,以外泌体的形式转运入内皮细胞,因而以 cPWWP2W 为靶点,针对周细胞 - 内皮细胞互作过程,可能是临床干预治疗糖尿病视网膜病变的新思路。
原文链接:https://www.pnas.org/content/116/15/7455.long
-END-


