小编这次要分享的两篇高分文献,是今年 5 月发表在 Gut 和 Mol Cancer 杂志的两篇文章,一个研究胃癌一个研究胰腺癌,都是很经典的研究套路。今天小编就为大家深度剖析文章思路,特别是就如何找到关键问题:怎么找到受甲基化酶调控的靶基因?做了具体的展示。
胃癌(Gastric cancer, GC) 是全球第五大常见肿瘤和第三大致命癌症,几乎一半的胃癌病例发生在东亚。大多数胃癌患者在晚期被诊断为恶性增生和转移。遗憾的是,晚期患者的预后非常糟糕。因此,识别新的生物标志物和治疗靶点对胃癌的诊断和治疗是迫切需要的。作者针对胃癌,展开 RNA m6A 修饰研究,从 METTL3 入手,上下游同时探索,成功探索到了完整的上下游作用机制。
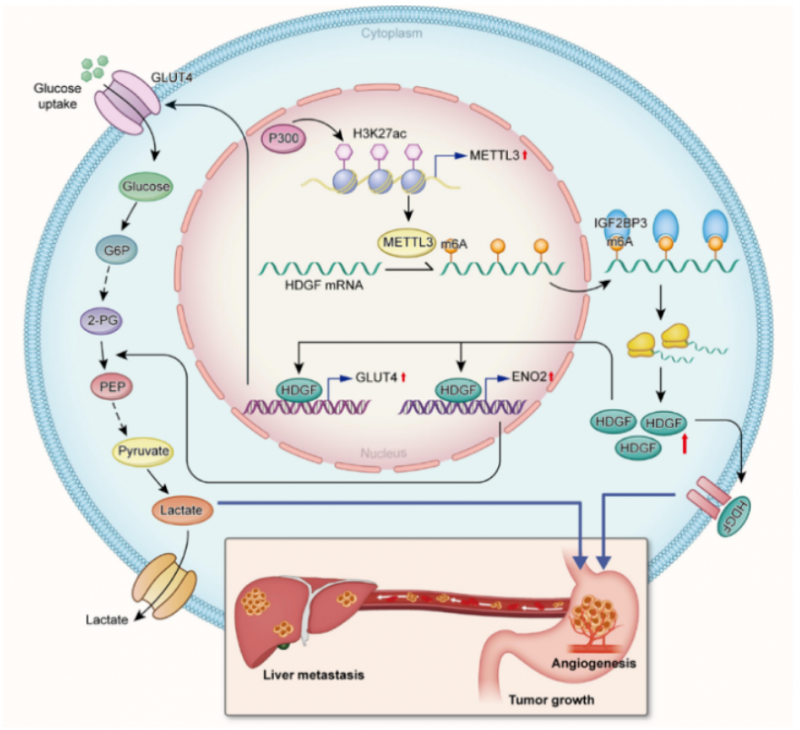
机制上,作者发现 p300 介导了 METTL3 在启动子区的 H3K27ac 修饰诱导了 METTL3 转录激活,METTL3 写入对 HDGF 基因的 m6A 修饰,IGF2BP3(reader)直接与 HDGF 上的 m6A 位点发生结合,维持该基因的稳定性。体内外实验证明 HDGF 的分泌促进肿瘤血管生成,而核内 HDGF 激活 GLUT4 和 ENO2 的表达,进而增加 GC 细胞的糖酵解,促进 GC 的进展,导致临床预后变差。
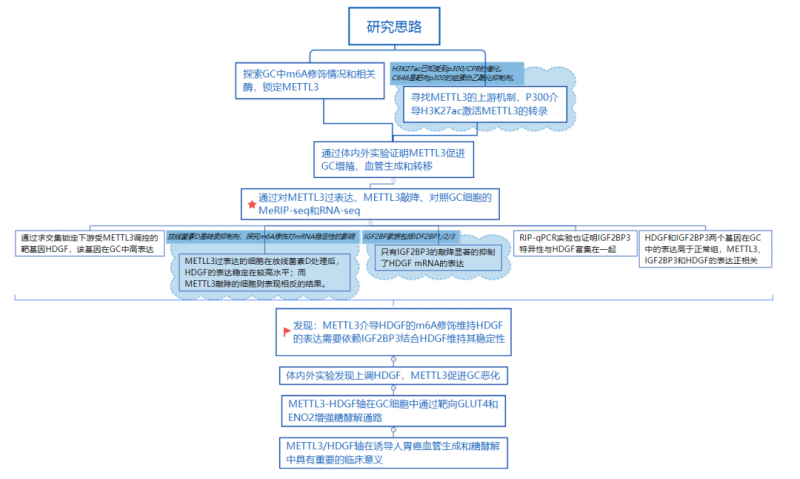
研究思路
关键结果
01、 研究 METTL3 的原因
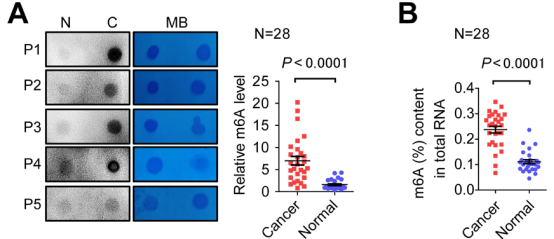
fig1AB 在 mRNA 和 total RNA 中 GC 的 m6A 整体水平显著高于正常组(N=28,14-14,pair)。
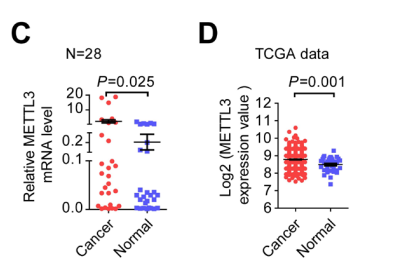
fig1CD qPCR 和 TCGA 结果发现 GC 的 METTL3 的表达水平显著高于正常组。
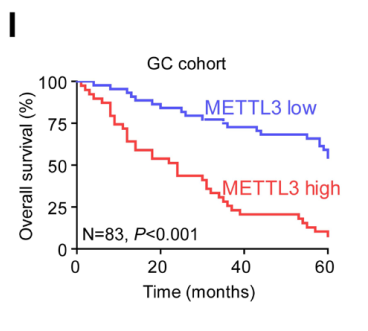
fig1I METTL3 的高表达与患者不良预后相关。
02、 探究 METTL3 上游的调控机制
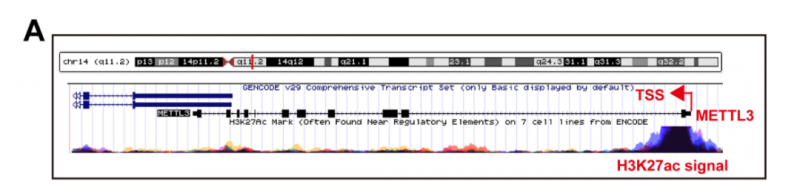
fig2A USCS 中 METTL3 启动子区存在 H3K27ac 修饰。

Fig2B 用 C646(C646 是靶向 p300 的组蛋白乙酰化抑制剂)处理不同类型细胞,对应的 METTL13 的表达水平降低。
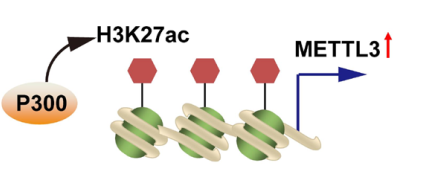
H3K27ac 已知受到 p300/CPB 的催化。H3K27ac 有助于 METTL3 的转录激活。
03、 通过 MeRIP-seq 挖掘下游受甲基化酶调控的机制
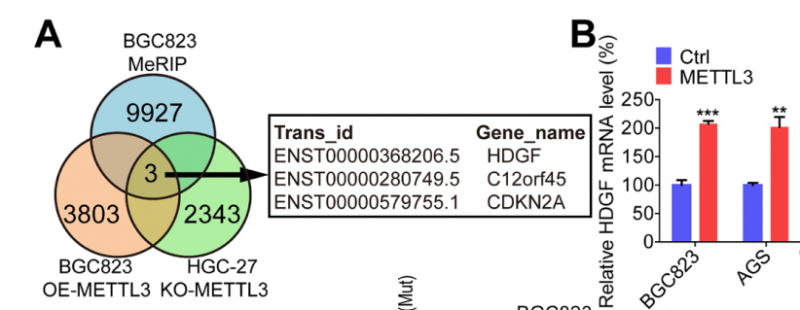
Fig5A 对 GC 模式细胞、KO METTL3 的 GC 模式细胞、过表达 METTL3 的 GC 模式细胞的 MeRIP-seq 和 RNA-seq 数据求交集,锁定下游靶基因 HDGF,METTL3 过表达的 GC 细胞中,对应 HDGF 表达也上调。

Fig5H METTL3 过表达的 MeRIP-seq 的 motif 结果提示,AGACC 序列在 HDGF 的外显子中序列中。
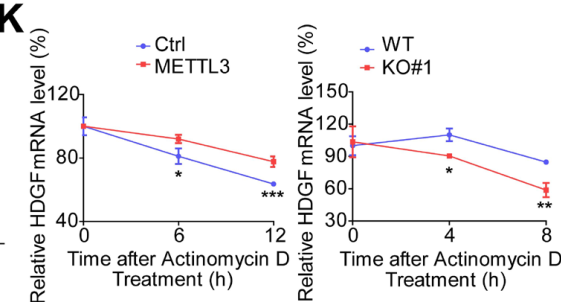
Fig5K 放线菌素 D(转录抑制剂)处理 GC 细胞在特定的时间段里。METLL3 过表达的细胞在处理后,HDGF 的表达稳定在较高水平;而 METTL3 敲除的细胞则表现相反的结果,说明 m6A 修饰会影响 HDGF 的稳定性。
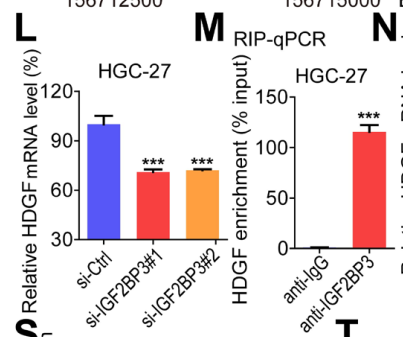
Fig5L 只有 IGF2BP3 的敲降显著的抑制了 HDGF mRNA 的表达。Fig5M RIP-qPCR 实验也证明 IGF2BP3 特异性与 HDGF 富集在一起。
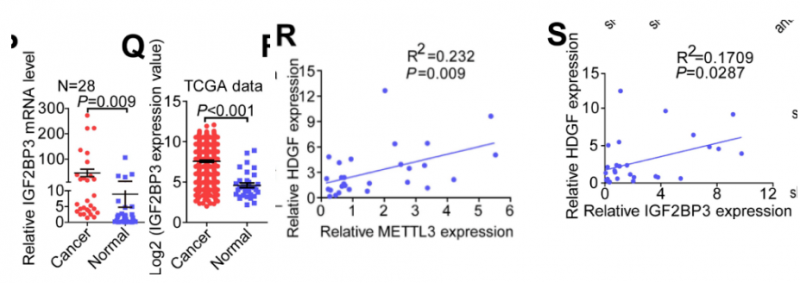
Fig5 OPQR. 在 TCGA 和 28 个样本中发现 HDGF 和 IGF2BP3 两个基因在 GC 中的表达高于正常组。3 个基因彼此正相关。
研究结论
揭示了 METTL3 在胃癌发展中的致癌作用。机制上,METTL3/ HDGF/GLUT4/ENO2 轴通过增加糖酵解和血管生成促进 GC 肿瘤发生和转移。此外,METTL3 在胃癌中表达明显升高,与胃癌患者预后不良相关。因此,METTL3 可能是胃癌潜在的预测因子和治疗靶点。此外该单位作者还同时发了一篇高分综述,围绕胃癌中的 RNA 甲基化酶 METTL3 展开,大家感兴趣可以自行下载。
胰腺癌是一种起病隐匿、早期诊断困难、手术切除率低的胃肠道恶性肿瘤,是世界上常见的致命肿瘤之一。胰腺癌的 5 年生存率仅为 8%,远处转移期甚至降至 3%。因此,迫切需要阐明胰腺癌的分子机制,以达到诊断和治疗干预的目的。作者针对胰腺癌,展开 RNA m6A 修饰研究,从 ALKBH5(eraser) 入手,上下游同时探索,成功探索到了上下游作用机制。思路其实和上篇差不多,都是先前期通过 TCGA 和自己的胰腺癌组织样本入手,发现 ALKBH5 存在显著差异。然后通过体内外实验来验证该基因对疾病的一个促进作用。关键的来了,对 ALKBH5 的过表达细胞和正常细胞进行 MeRIP-seq 和 RNA-seq,然后做差异分析,求交集,就能基本锁定受甲基化酶调控的基因(PER1)。
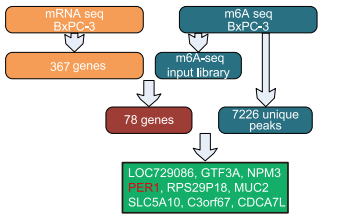
上图就是作者可视化了如何筛选到受甲基化酶调控靶基因的过程
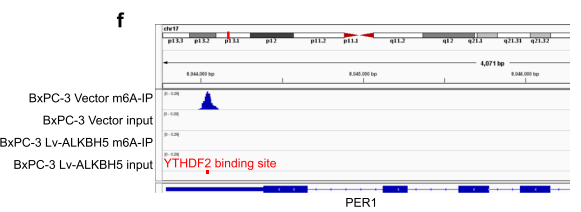
ALKBH5 过表达后,PER1 的 3’UTR 区的 m6A 修饰被擦除。
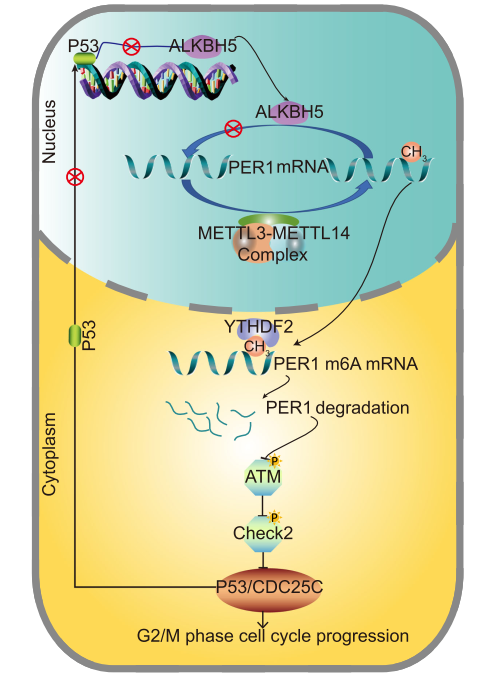
机制上,ALKBH5 通过转录后调控 m6A 去甲基化作用以 m6A- YTHDF2 依赖的方式激活 PER1。PER1 的上调导致 ATM-CHK2-P53/CDC25C 信号通路的重新激活,抑制细胞生长。p53 诱导的 ALKBH5 转录激活在胰腺癌中起着调节 m6A 修饰的反馈回路作用。
文末是小编收集的近几个月的较高分有关 m6A 修饰的研究,感兴趣的老师可以联系在线客服沟通 获取。
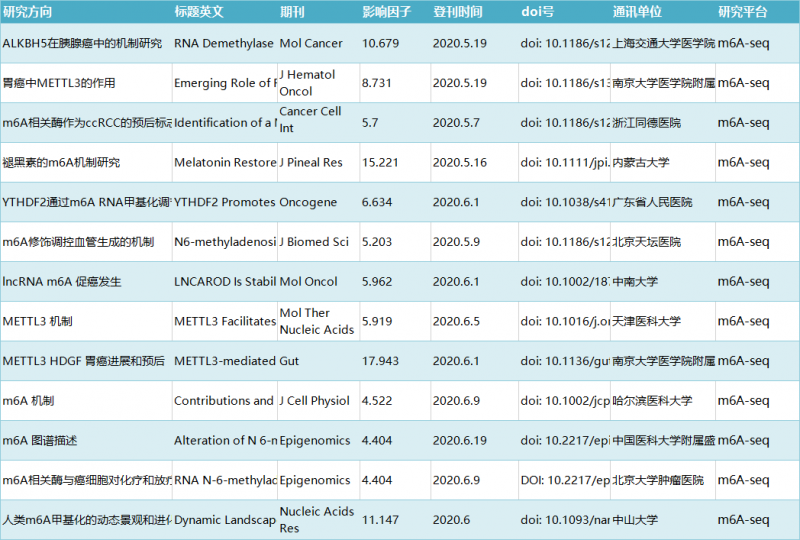
更多伯豪生物服务

